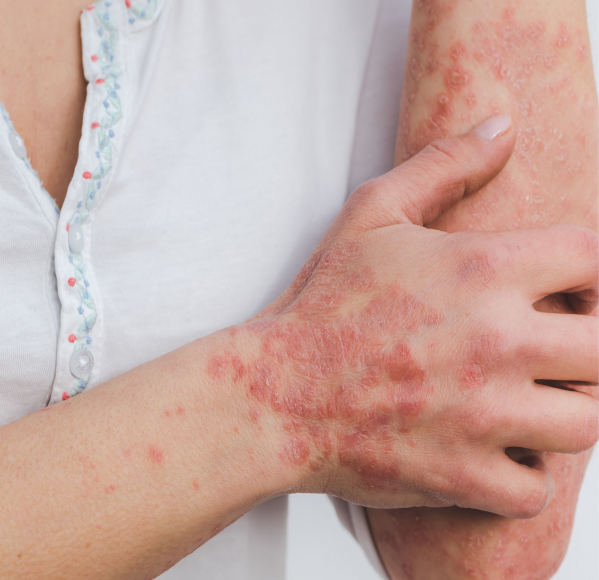
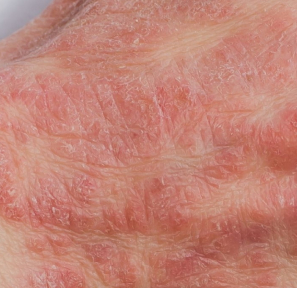
también conocido como dermatitis atópica, es una afección de la piel no contagiosa que puede afectar a personas de todas las edades. El eccema puede ser de leve a grave y a menudo se caracteriza por piel enrojecida, con picazón, seca y agrietada.
Las zonas del cuerpo afectadas con frecuencia incluyen la cara, el interior de los codos o detrás de las rodillas, pero el eccema puede aparecer en cualquier parte del cuerpo¹. Durante una “exacerbación”, los síntomas pueden llegar a ser dolorosos con un aumento de la necesidad de rascarse, lo que provoca cambios en el color de la piel y la aparición de ampollas sangrantes en carne viva. Se desconoce la causa exacta del eccema, pero puede aparecer debido a una combinación de genes y desencadenantes individuales². Entre algunos ejemplos de desencadenantes se pueden incluir: alérgenos, cosméticos, detergentes, determinados tejidos, cambios en el clima (especialmente aire seco) e incluso el estrés.
Los médicos que participan en el estudio clínico EASE están probando un fármaco en investigación (EP262) para estudiar su seguridad, tolerabilidad y efectos en pacientes con eccema.
El eccema puede desarrollarse debido a una combinación de factores genéticos y ambientales, lo que provoca una disfunción de la barrera cutánea y un desorden del sistema inmunitario. Los mastocitos (un tipo de célula inmunitaria presente en la piel) han tenido participación en el desarrollo de lesiones cutáneas por eccema y en su gravedad³. MRGPRX2 es uno de los receptores de los mastocitos, y la activación de MRGPRX2 puede incidir en el eccema. EP262 es un medicamento experimental diseñado para bloquear los activadores del receptor MRGPRX2, lo que puede resultar en menor cantidad de lesiones o lesiones menos graves.
EP262 representa un nuevo enfoque dirigido al tratamiento del eccema que solo está disponible mediante la participación en un estudio clínico.
Si tiene eccema, puede que le interese obtener más información sobre el estudio EASE.